モルモットを用いる皮膚感作性試験として,最も広く行われている方法がMagnusson and Kligmanによって開発されたMaximization testである1)。この試験方法は,動物を用いた遅延型アレルギー反応を調べるものとして,国内「医薬品毒性試験法ガイドライン」2),「医療用具及び医用材料の基礎的な生物学的試験のガイドライン」3)や,ISO基準「医用材料の生物学的評価」(10993-10) 4)等に掲載されている。
ガイドラインによって投与検体の調製法などに違いがあるが,ここでは,医薬品ガイドラインの内容を基本に置いて述べる。
B. 実験材料等
1. 動物
通常500g以下の健康な若齢白色モルモット (1〜3ヶ月齢) が用いられる。雌雄どちらでも使用可能であるが,雌を使用する場合は,妊娠していない未経産のものを用いる。
2. 動物数
通常,被験物質投与群に10匹,陰性 (溶媒) 対照群に5匹用意する。国内の申請資料として用いる場合には,陽性対照群 (5匹) を設定する必要がある。
3. 陽性対照物質
陽性対照物質として,次のような物質が用いられている。
1-chloro-2,4-dinitrobenzene (DNCB, CAS No.97-00-7),potassium di-chromate (CAS No.7778-50-9),p-phenylenediamine (CAS No.106-50-3),neomycin culfate (CAS No. 1405-10-3),nickel sulfate (CAS No. 7786-81-4)。
4. 試薬
1) Freund's Complete Adjuvant (FCA)
2) 蒸留水 (局方注射用水)
3) 10%ラウリル硫酸ナトリウム(SLS)のワセリン軟膏:ワセリンを加温融解したところに1/10量(w/w)のSLSを加え,均一な軟膏とする。
4) 被験物質溶解用溶媒 (感作投与用と惹起投与用)
5. 器具
1) ルアーロック付きガラスシリンジ (10mL) をポリエチレンチューブでつないだもの:2組 あるいはホモジナイザー
2) 皮内投与用ガラスシリンジ (1〜2mL) およびディスポシリンジ
3) 感作貼付用パッチ:FRPフィルムなどで裏打ちしたろ紙 (約2×4cm) を動物数分
4) 惹起貼付用パッチ:FRPフィルムなどで裏打ちしたリント布( 約1.5×1.5cm) あるいはフィンチャンバー (内径8mm) を必要数
5) 粘着性伸縮包帯
6) 動物用バリカン
7) シェーバー
8) マイクロピペット,チップ
C. 実験操作手順
1.投与試験液の調製
1) 蒸留水とFCAとの1:1の油中水型(W/O)乳化物の作製
蒸留水を入れたガラスシリンジと等量のFCAを入れたガラスシリンジをフランジを介してポリエチレンチューブで接合し,一方から他方へ交互に混合液を往復させる操作を繰り返す。この操作により,液の粘稠度が高まり,内筒を押すのに抵抗が生じ,かつ液が白濁してくる。水に一滴たらして,拡散しなければ混和は完全である。ガラスシリンジの代わりにホモジナイザーを用いても良い。
2) 被験物質溶液を調製
予め被験物質を溶解するための溶媒を検討しておく。感作皮内投与のためには,蒸留水や生理食塩液,オリーブ油など刺激性の少ないものを,惹起投与のためには,揮発性が高く,かつ刺激性のない溶媒 (エタノール,アセトンなど) を選択する。溶媒には,それ自身が感作性を有するものもあるので,感作用と惹起用の溶媒は別種にした方が良い。予め予備試験を行い,それぞれの溶媒および投与経路において,被験物質溶液が刺激性を示さない最高濃度を調べておく。予備試験によって決定した濃度 (皮内投与によって刺激性を示さない最高濃度) の被験物質溶液を調製する。
3) 被験物質とFCAとの混合物の調製
2)で調製した被験物質溶液の2倍濃度の溶液とFCAの等量混合乳化物を調製する。2)の溶媒が水系でない場合には,単に混合しただけの均一な溶液のままでも良いが,その混合液に蒸留水を少し加えて,乳化物を作製しても良い。
2. 感作
1) 皮内投与の前日に肩甲骨上部皮膚の毛を刈っておく。2×4cmの区画を3つの部位 (図参照) に分け,下記に示した試験液をそれぞれ0.1mLずつ,左右対称に皮内投与する。
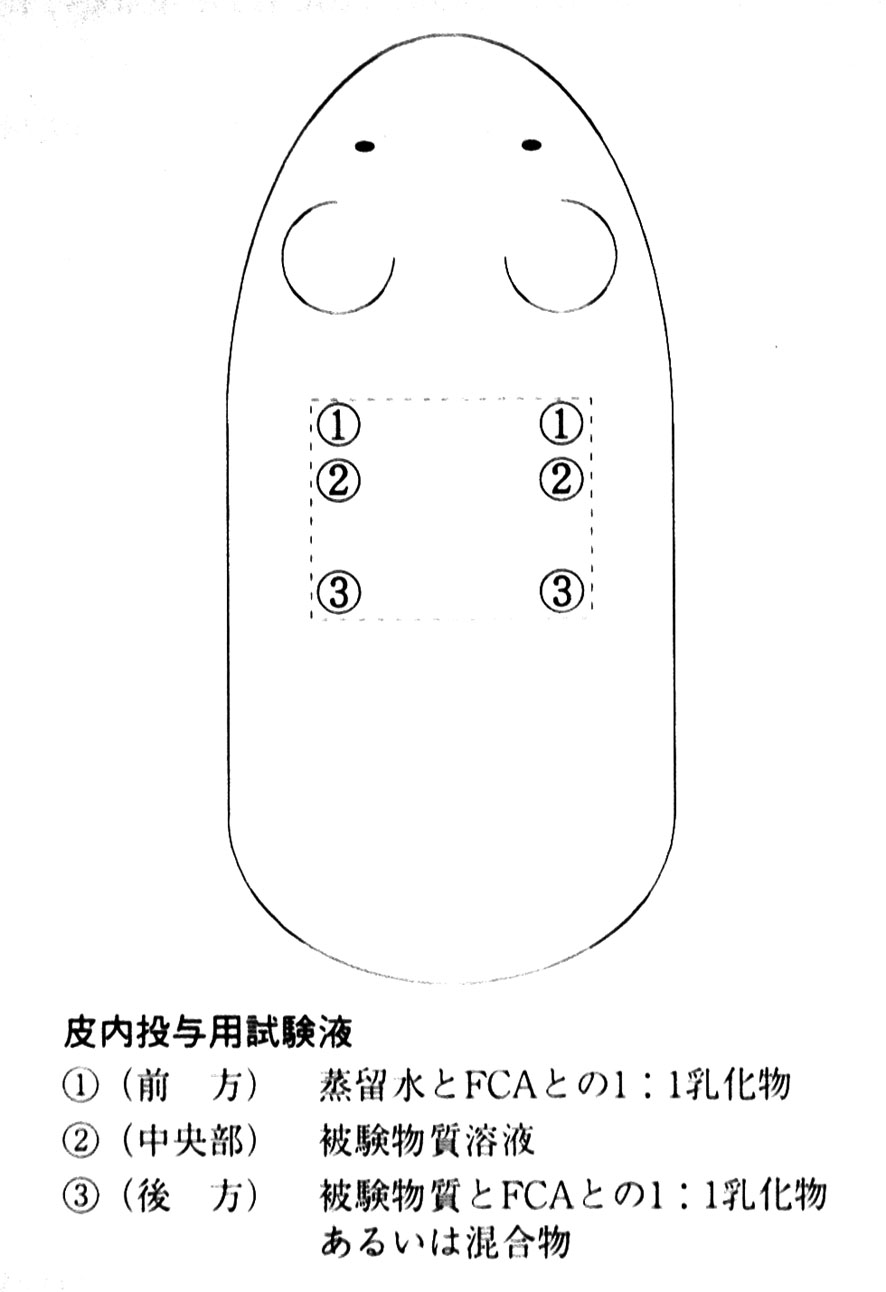
2) 感作皮内投与の7日後,あらかじめ剪毛および剃毛しておいた皮内投与部位に10%SLS軟膏を開放塗布する。翌日,SLSを拭き取った後,下記に示した試験液をそれぞれ0.2mLずつ,感作貼付用パッチおよび粘着性伸縮包帯を用いて48時間閉塞貼付する。
感作貼付用試験液 1) ②の溶液
3. 惹起
感作貼付開始日から2週間後に,あらかじめ剪毛および剃毛しておいた左右側腹部あるいは背部に,以下に示した試験液 (段階希釈溶液と溶媒対照) をそれぞれ0.1mLずつ惹起用パッチに吸収させて24時間閉塞あるいは開放適用する。
惹起用試験液
刺激性を示さない最高濃度から段階希釈した被験物質溶液および溶媒対照液
D. 評価
開放適用後,24時間および48時間,閉塞適用の場合は貼付物剥離後24時間および48時間における各塗布部位の皮膚反応を観察し,以下に示したDraizeの判定基準に基づいて判定する。